HyperScript™ First-Strand cDNA Synthesis Kit
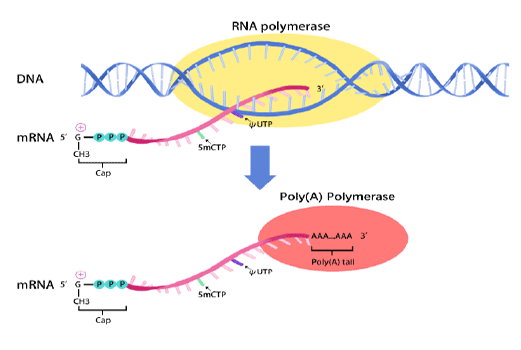
mRNA synthesis
In vitro transcription of capped mRNA with modified nucleotides and Poly(A) tail
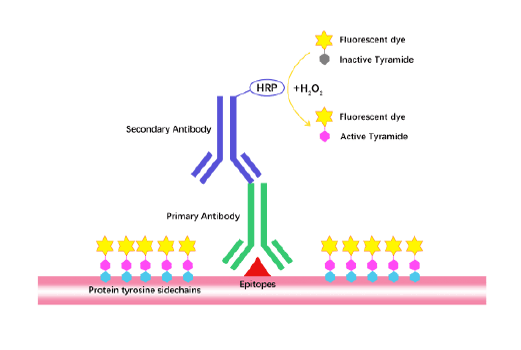
Tyramide Signal Amplification (TSA)
TSA (Tyramide Signal Amplification), used for signal amplification of ISH, IHC and IC etc.
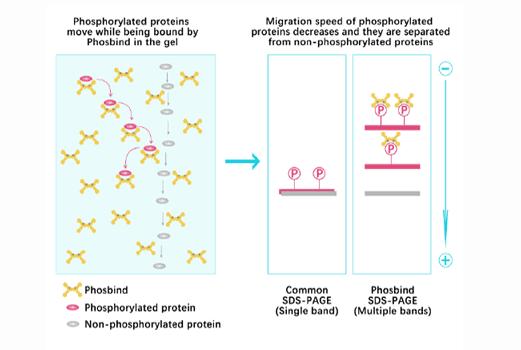
Phos Binding Reagent Acrylamide
Separation of phosphorylated and non-phosphorylated proteins without phospho-specific antibody
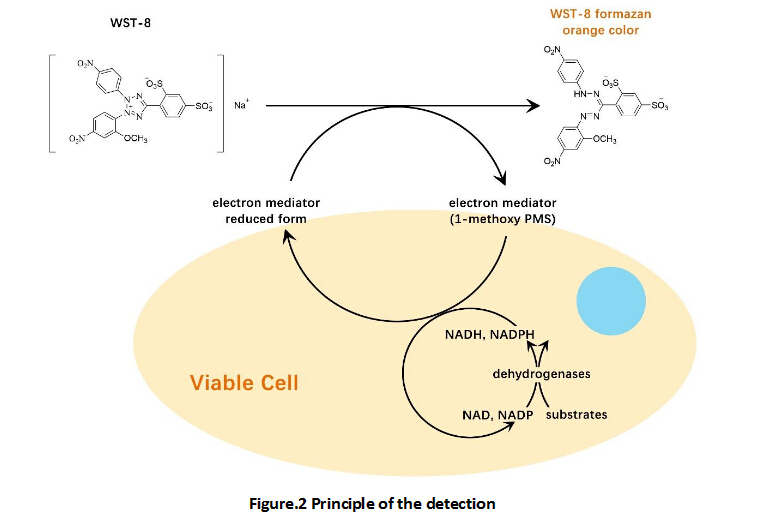
Cell Counting Kit-8 (CCK-8)
A convenient and sensitive way for cell proliferation assay and cytotoxicity assay
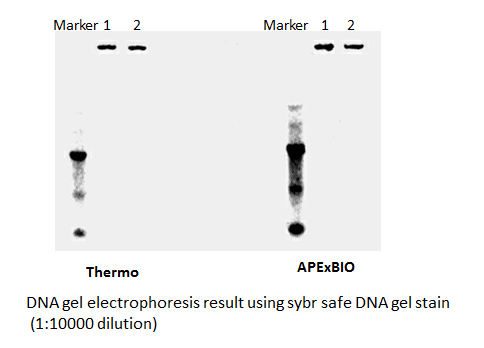
SYBR Safe DNA Gel Stain
Safe and sensitive stain for visualization of DNA or RNA in agarose or acrylamide gels.
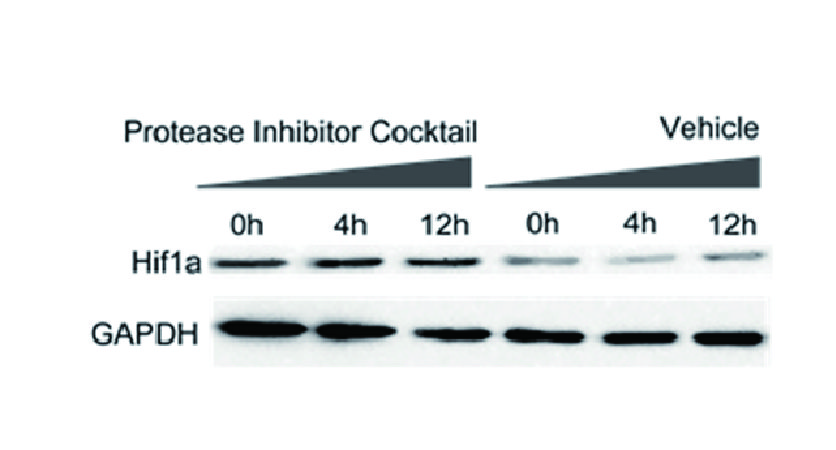
Inhibitor Cocktails
Protect the integrity of proteins from multiple proteases and phosphatases for different applications.
- 1. Bing Li, Ge Lou, et al. "Repression of lncRNA PART1 attenuates ovarian cancer cell viability, migration and invasion through the miR-503-5p/FOXK1 axis." BMC Cancer. 2022 Jan 31;22(1):124. PMID: 35100978
- 2. Hongrong Wang, Shasha Song, et al. "Long non-coding RNA HOTAIR knockdown alleviates lipopolysaccharide-induced acute respiratory distress syndrome and the associated inflammatory response by modulating the microRNA-30a-5p/PDE7A axis." Exp Ther Med. 2021 Oct;22(4):1160. PMID: 34504605
- 3. Yu-Qing Pan, Min Niu, et al. "Effect of MT2A on apoptosis and proliferation in HL60 cells." Int J Med Sci. 2021 Jun 4;18(13):2910-2919. PMID: 34220318
- 4. Yonglei Liu, Lixia Wang, et al. "Ramelteon Ameliorates LPS-Induced Hyperpermeability of the Blood-Brain Barrier (BBB) by Activating Nrf2." Inflammation. 2021 Oct;44(5):1750-1761. PMID: 33876343
HyperScript™ First-Strand cDNA Synthesis Kit是基于HyperScript™ Reverse Transcriptase(货号:K1071)从Total RNA或Poly(A)+RNA合成第一链cDNA的试剂盒。HyperScript™ Reverse Transcriptase是在M-MLV (RNase H-) Reverse Transcriptase基础上经过基因工程改造后获得的全新逆转录酶,相较而言HyperScript™ Reverse Transcriptase降低了RNase H活性且大幅度提高了热稳定性。HyperScript™ Reverse Transcriptase可耐受更高的反应温度,适用于具有复杂二级结构的RNA模板的逆转录。此外,HyperScript™ Reverse Transcriptase增强了与模板的亲和力,适合少量模板以及低拷贝基因的逆转录,可合成长达12.3 kb的第一链cDNA。
HyperScript™ First-Strand cDNA Synthesis Kit包含合成第一链cDNA所需的所有组分,并提供Random Primers和Oligo (dT)23VN 两种cDNA合成引物。可根据实验需要选择Random Primers、Oligo (dT)23VN或基因特异性引物作为逆转录引物,合成的第一链cDNA产物可用于后续的PCR扩增、qPCR反应等实验。
基于高效的HyperScript™ Reverse Transcriptase,适用于具有二级结构的RNA 模板
合成第一链cDNA片段可长达12.3 kb
可检测低至1 pg的模板起始量
Kit中提供的Oligo (dT)23VN引物比Oligo (dT)18对模板锚定能力更强,逆转录效率更高
合成的第一链cDNA 可用于PCR 扩增、qPCR 反应等实验
| 组分 | 20 rxn(20 μL reaction) | 50 rxn(20 μL reaction) | 100 rxn(20 μL reaction) |
| HyperScript™ Reverse Transcriptase (200 U/μL) | 20 μL | 50 μL | 100 μL |
| 5X First-Strand Buffer | 80 μL | 200 μL | 400 μL |
| RNase Inhibitor, Murine(40 U/μL) | 20 μL | 50 μL | 100 μL |
| 10 mM dNTP Mixture | 20 μL | 50 μL | 100 μL |
| RNase Free ddH2O | 1 mL | 1 mL | 1 mL x 2 |
| Random Primers (50 μM) | 20 μL | 50 μL | 100 μL |
| Oligo (dT) 23VN (50 μM) | 20 μL | 50 μL | 100 μL |
所有组分储存于-20°C。 | |||
1)Q:收到产品后应怎么保存?
A:所有组分-20°C保存,有效期至少1年。
2)Q:能否通过延长逆转录时间来提高逆转录效率?
A:对于大多数基因,延长逆转录时间对逆转录效率并没有明显的提升;但对于一些GC含量较高或含高级复杂结构的模板,延长逆转录时间可提升逆转录效率。
3)Q:原核生物RNA能否用该逆转录酶?
A:可以。因为原核生物的RNA没有poly A尾,在逆转录反应体系中需要选择Random primer作为逆转录引物。
4)Q:逆转录反应引物如何选择?
A:常用引物类型包括:随机引物、Oligo dT和基因特异性引物,选择情况如下:
a. 随机引物:随机结合在RNA的任何区域,适用于rRNA、mRNA、tRNA等所有RNA类型的逆转录反应。
b. Oligo dT:适用于具有Poly A尾的RNA(原核生物RNA、真核生物的rRNA和tRNA是不具有PolyA尾的)。由于Oligo dT结合在PolyA尾上,所以对RNA样品的质量要求较高,即使有少量的降解也会使全长cDNA合成量大大减少。
c. 基因特异性引物:与模板序列互补,适用于序列已知的基因逆转录。
当cDNA后续是用于qPCR实验时,一般使用Oligo dT和随机引物的混合物,可以避免3’端和5’端的扩增偏好性;当cDNA后续是用于PCR扩增长片段时,一般用Oligo dT或者基因特异性引物,不建议使用随机引物。因为随机引物是随机结合的,cDNA片段会偏短,可能会对长片段扩增造成稀释,后续扩增不出全长的目的基因。
5)Q:可以通过测逆转录产物cDNA的浓度来判定逆转录的效率吗?
A:可以通过测逆转录产物cDNA的浓度来判定逆转录的效率吗?
6)Q:逆转录产物用PCR扩增后跑胶检测无特异性条带?
A:可能原因及解决方案如下:
a. 引物设计欠佳或逆转录产物质量欠佳:可先使用actin、GAPDH等作为内参进行PCR扩增,看是否可以成功扩增。如果内参不能被很好地扩增,则有可能PCR引物存在问题或逆转录产物质量欠佳。
b. 模板RNA发生了降解:哺乳动物细胞或组织的总RNA琼脂糖电泳后应该可以看到清晰的18S和28S rRNA条带,并且28S rRNA和18S rRNA的亮度比例应该大于等于2.0,如果比例小于2.0,则说明总RNA发生了显著的降解,需重新制备模板。
c. 模板RNA的纯度偏低:在提取纯化RNA的过程中,残留在溶液中的一些成分如苯酚、SDS、EDTA等会抑制逆转录酶活性。可对RNA样品进行柱纯化,或者进行沉淀、洗涤和再溶解,通常可以有效去除残留的污染物。
d. 逆转录模板量不足:在抽提获得总RNA后,在进行一些精细的定量检测时通常会进行DNase I消化,以充分去除可能的残留的DNA的干扰。DNase I进行热失活时,需要加入EDTA至终浓度为2.5mM,否则RNA在没有螯合剂的情况下,在加热过程中容易被水解,从而导致模板量不足。此外,扩增特定基因时,需要先查询该基因的组织分布特点,利用其高表达的组织进行目的基因的反转录和克隆。
e. 逆转录引物类型选择不当:对于细菌RNA和不含poly A尾的RNA,要用随机引物代替Oligo(dT)引物。使用基因特异性引物时,需要确保基因特异性引物设计合理正确。
f. RNA模板富含GC或容易形成二级结构:可考虑把反转录温度提高到45-55℃。


